An zahlreichen Standorten in der DACH-Region werden weiterhin neue Labor- und Produktionskapazitäten geplant oder umgesetzt. Gleichzeitig rückt die Frage nach nachhaltigen, wirtschaftlich tragfähigen Konzepten stärker in den Fokus. Auch die clusterverbindende Kooperation wird ein größeres Thema.
Europa versus USA versus oder mit China. Die klinische Entwicklung von Wirkstoffen in der DACH-Region, in Europa, steht vor einer Reihe struktureller und operativer Herausforderungen.
BioVersys kooperiert exklusiv mit dem US-Netzwerk Hackensack Meridian Health zur Entwicklung neuer Ansamycin-Antibiotika gegen schwer behandelbare Nicht-Tuberkulose-Mykobakterien-Infektionen. Die Partnerschaft stärke die Pipeline und ziele auf wirksamere, oral verfügbare Therapien für chronische Lungenpatienten. HMH erhält Zahlungen und Umsatzbeteiligungen.
Das Medizintechnikunternehmen Siemens Healthineers stärkt mit 250.000 Euro die Forschung am Uniklinikum Erlangen. Das Geld fließt in die Namensstiftung „Foundation for Sustainable Healthcare“ und ist gleichzeitig ein Bekenntnis zum Standort Erlangen.
Gen- und Zelltherapie sind Hoffnung für viele Betroffene. Sie stehen aber auch vor großen Herausforderungen in der Entwicklung und Herstellung. Ein Zusammenspiel vieler Akteure ist für den Erfolg unerlässlich.
Die analytica 2026 verzeichnet mehr Aussteller und Besucher und bestätigt ihre Rolle als internationaler Branchentreff. Im Fokus standen vor allem KI, Automatisierung und digitale Labore. Rund 35.000 Teilnehmer informierten sich in München über aktuelle Entwicklungen in Analytik, Labortechnik und Biotechnologie. China ist ein Thema, doch wegen stagnierender Zahlen dominiert eher der Wunsch der Laborausrüster, wieder mehr Aufmerksamkeit in Gesellschaft und Politik zu erhalten.
In der biomedizinischen Forschung hat cell free DNA (cfDNA) in den letzten Jahren stark an Bedeutung gewonnen, da sie einen minimal invasiven Zugang zu genetischen Informationen ermöglicht.
Mit einer neuen Baukastenmethode aus Genf eröffnen Forscher Möglichkeiten zur über bestimmte Zelloberflächenmarker zielgerichteten zellulären Adressierung von Wirkstoffen, ohne dabei einen Antikörper zu benötigen. Über eine Hybridization Chain Reaction (HCR) genannte Methode wird das Effektormolekül nur wirksam zusammengesetzt, wenn die ausgewählten unterschiedlichen Biomarker auch wirklich gemeinsam auf einer Zelle vorhanden sind.
Novartis kauft wieder ein und die kalifornische Excellergy für bis zu 2 Mrd. Dollar. Der Antikörper Exl-111 soll die Allergie-Pipelinestärken und über den bisherigen Standard hinausgehen. Der Deal ist Teil einer Serie von Zukäufen, mit denen der Konzern seine Innovationsbasis gezielt ausbaut.



 Michael Rabenstein/Uniklinikum Erlangen
Michael Rabenstein/Uniklinikum Erlangen

 Messe München
Messe München
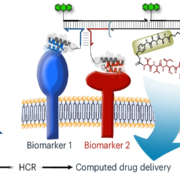 Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0
Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0 Novartis
Novartis